備受矚目的數據安全發展大會在浙江溫州隆重召開。本次大會以“筑牢數據安全屏障,賦能數字經濟發展”為主題,匯聚了來自全國各地的政府代表、行業專家、企業領袖及學術研究者,共同探討數據安全領域的前沿趨勢、技術創新與產業實踐,為構建安全、可信、高效的數據要素市場獻計獻策。
大會的核心焦點之一,是再次將全國的目光引向了“中國(溫州)數安港”這一重要的數字基礎設施與產業集聚平臺。自啟動建設以來,溫州數安港以打造國家級數據安全與合規流通樞紐為目標,積極探索數據要素市場化配置改革路徑,致力于提供安全可靠的數據處理、存儲、交易和應用服務。此次大會上,數安港的最新建設成果、創新運營模式以及系列重磅合作項目的發布,充分展示了其在推動數據安全技術落地、促進數據產業生態繁榮方面的關鍵作用與引領價值。
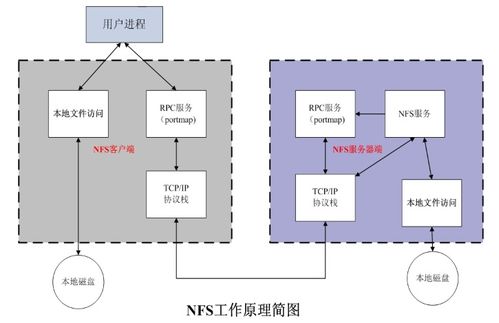
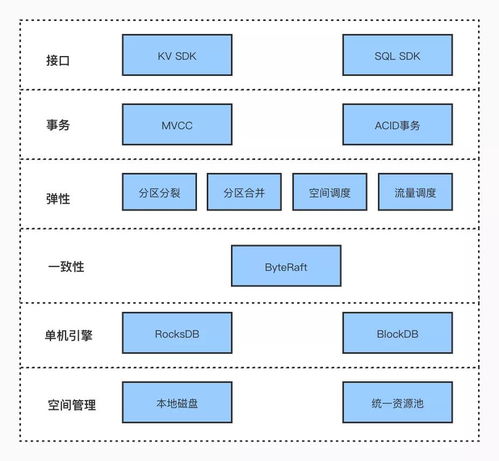
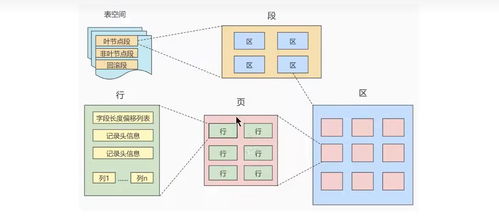
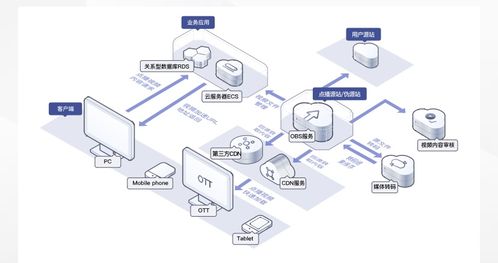
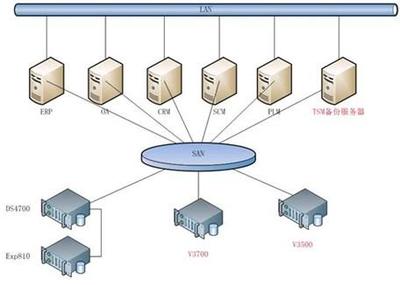
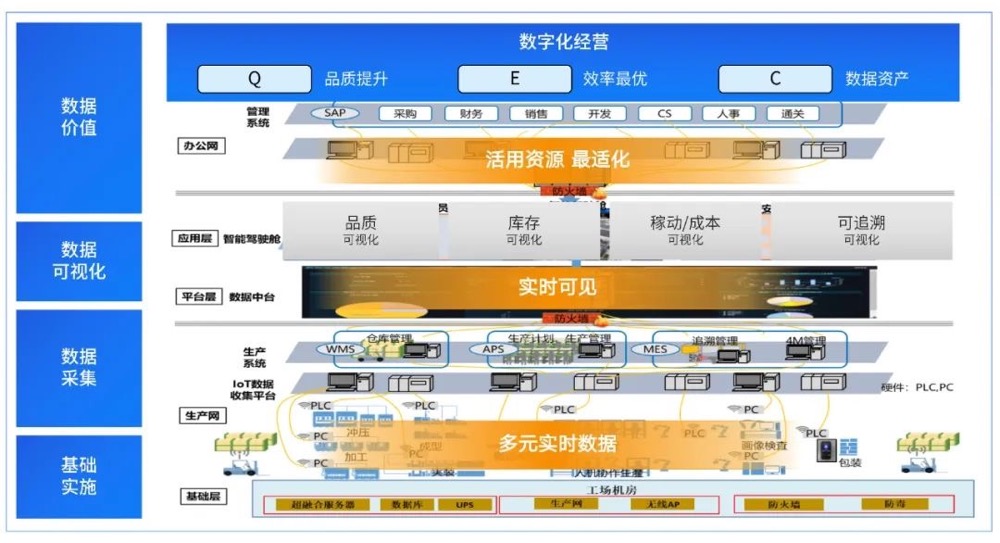
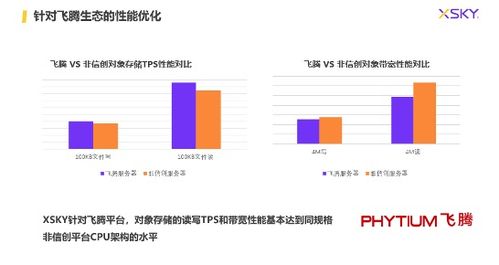
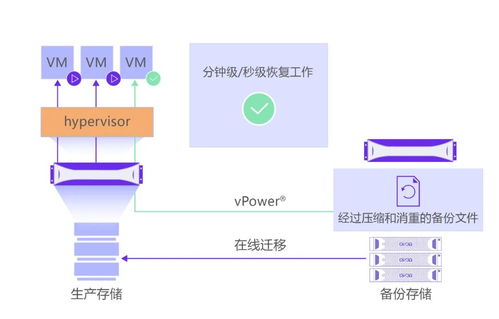
與會專家指出,在數字經濟成為全球經濟增長新引擎的背景下,數據作為關鍵生產要素,其安全與合規利用的重要性日益凸顯。數據處理和存儲服務作為數據價值鏈的基礎環節,面臨著技術、法規、管理等多重挑戰。本次大會深入研討了隱私計算、區塊鏈、可信硬件等前沿技術在保障數據全生命周期安全中的應用,分析了《數據安全法》、《個人信息保護法》等法律法規框架下的合規要求與實踐,并分享了企業在構建彈性安全架構、實現數據分類分級保護、應對新型網絡威脅等方面的成功經驗。
“中國(溫州)數安港”的實踐,為全國提供了可借鑒的樣本。它通過建設高標準的數據中心集群,引入和培育一批專注于數據安全技術研發、數據治理服務、數據價值挖掘的創新企業,并積極搭建政、產、學、研、用協同平臺,旨在形成覆蓋數據采集、存儲、處理、流通、應用、銷毀各環節的安全能力閉環。這不僅為溫州及長三角區域的產業數字化轉型提供了堅實支撐,也為全國數據要素市場的健康、有序發展貢獻了“溫州智慧”與“溫州方案”。
隨著數據安全發展大會的成功舉辦和“中國(溫州)數安港”影響力的持續提升,溫州有望進一步鞏固其在國家數據安全與產業發展格局中的戰略支點地位。持續深化技術創新、完善制度規范、優化產業生態,將成為推動數據處理和存儲服務邁向更安全、更高效、更智能新階段的關鍵,從而為數字經濟高質量發展注入源源不斷的強大動能。